อะตอม
จากวิกิพีเดีย สารานุกรมเสรี
| อะตอม | ||||||
|---|---|---|---|---|---|---|
 | ||||||
| แบบจำลองอะตอมของฮีเลียม (ไม่ใช่อัตราส่วนจริง) ภาพนิวเคลียสซึ่งมีโปรตอน 2 ตัว (สีแดง) นิวตรอน 2 ตัว (สีเขียว) และ กลุ่มควันแสดง ความน่าจะเป็นของตำแหน่ง (สีเทา) ของอิเล็กตรอน (สีเหลือง) | ||||||
| ประเภท | ||||||
| ||||||
| คุณสมบัติ | ||||||
|
- สำหรับศิลปินจากรายการไมค์ไอดอล (อะตอม ไมค์ไอดอล) ดูที่ กฤชกนก สวยสด
คำว่า อะตอม มาจากภาษากรีกว่า ἄτομος/átomos, α-τεμνω ซึ่งมีความหมายว่า ไม่สามารถแบ่งได้อีกต่อไป หลักการของอะตอมในฐานะส่วนประกอบเล็กที่สุดของสสารที่ไม่สามารถแบ่งได้อีก ต่อไปเสนอขึ้นครั้งแรกโดยนักปรัชญาชาวอินเดียและนักปรัชญาชาวกรีก ในคริสต์ศตวรรษที่ 17-18 นักเคมีเริ่มวางแนวคิดทางกายภาพจากหลักการนี้โดยแสดงให้เห็นว่าวัตถุหนึ่งๆ ไม่สามารถแบ่งแยกได้อีกต่อไปด้วยกระบวนการทางเคมี ระหว่างช่วงปลายคริสต์ศตวรรษที่ 19 และต้นคริสต์ศตวรรษที่ 20 นักฟิสิกส์ค้นพบส่วนประกอบย่อยของอะตอมและโครงสร้างภายในของอะตอม ซึ่งเป็นการแสดงว่า "อะตอม" ยังสามารถแบ่งแยกได้ หลักการของกลศาสตร์ควอนตัมเป็นหลักการที่นำมาใช้สร้างแบบจำลองทางคณิตศาสตร์ของอะตอมได้เป็นผลสำเร็จ[2][3]
ตามความเข้าใจในปัจจุบัน อะตอมเป็นวัตถุขนาดเล็กมากที่มีมวลน้อยมากๆ เราสามารถสังเกตการณ์อะตอมเดี่ยวๆ ได้โดยอาศัยเครื่องมือพิเศษ เช่น scanning tunneling microscope มวลประมาณ 99.9% ของอะตอมจะกระจุกรวมกันอยู่ในนิวเคลียส[note 1] โดยมีโปรตอนและนิวตรอนเป็นมวลที่เหลือประมาณเท่าๆ กัน ธาตุแต่ละตัวจะมีอย่างน้อยหนึ่งไอโซโทปที่มีนิวเคลียสซึ่งไม่เสถียรและเกิด การเสื่อมสลายโดยการแผ่รังสี ซึ่งเป็นสาเหตุให้เกิดการแปลงรูปทางนิวเคลียร์ที่ทำให้จำนวนโปรตอนและนิวตรอนในนิวเคลียสเปลี่ยนแปลงไป[4] อิเล็กตรอนที่โคจรรอบอะตอมจะมีระดับพลังงานที่เสถียรอยู่จำนวนหนึ่งในลักษณะของวงโคจรอะตอม และสามารถเปลี่ยนแปลงระดับไปมาระหว่างกันได้โดยการดูดซับหรือปลดปล่อยโฟตอนที่ สอดคล้องกับระดับพลังงานที่ต่างกัน อิเล็กตรอนเหล่านี้เป็นตัวกำหนดคุณสมบัติทางเคมีของธาตุ และมีอิทธิพลอย่างมากต่อคุณสมบัติทางแม่เหล็กของอะตอม
อนุภาคหลักที่พบได้ในอะตอมทั่วไปมี 3 ชนิด คือ
- โปรตอน มีประจุบวก อยู่ในส่วนนิวเคลียสเป็นแกนกลางของอะตอม
- นิวตรอน ซึ่งไม่มีประจุ น้ำหนักใกล้เคียงกับโปรตอน ในอะตอมบางชนิดไม่มีนิวเคลียส เช่นอะตอมของโปรเทียม (ไอโซโทปหนึ่งของไฮโดรเจน)
- อิเล็กตรอน มีประจุลบ เบากว่าอนุภาคทั้งสองชนิดแรกมาก เคลื่อนที่อย่างรวดเร็วอยู่รอบนิวเคลียส
นอกจากธาตุที่เกิดตามธรรมชาติแล้ว ยังมีธาตุที่ถูกสร้างขึ้น แต่ธาตุเหล่านี้มักจะไม่เสถียร และ สลายไปเป็นธาตุอื่นที่เสถียร โดยกระบวนการสลายกัมมันตรังสี ตัวอย่างเช่น Beta Decay, Double Beta Decay, Beta Capture, Gamma Decay และอื่น ๆ
ถึงแม้ว่าจะมีธาตุที่เกิดตามธรรมชาติเพียง 90 ชนิด อะตอมของธาตุเหล่านี้สามารถสร้างพันธะเคมี รวมกันเป็นโมเลกุล และองค์ประกอบชนิดอื่นๆ โมเลกุลเกิดจากการรวมตัวกันของอะตอมหลายอะตอม เช่น โมเลกุลของน้ำเกิดจากการรวมตัวกันของอะตอมไฮโดรเจน 2 อะตอม และ อะตอมออกซิเจน 1 อะตอม
เนื่องจากอะตอมเป็นสิ่งที่มีอยู่ไปทั่วทุกที่ จึงเป็นหัวข้อศึกษาที่ได้รับความสำคัญในหลายศตวรรษที่ผ่านมา หัวข้อวิจัยทางด้านอะตอมในปัจจุบันจะเน้นทางด้าน quantum effects เช่น ของเหลวผลควบแน่นโบส-ไอน์สไตน์
ประวัติ
[แก้] แนวคิดเรื่องอะตอม
การอ้างอิงถึงแนวคิดอะตอมยุคแรกๆ สืบย้อนไปได้ถึงยุคอินเดียโบราณในศตวรรษที่ 6 ก่อนคริสตกาล[6] โดยปรากฏครั้งแรกใน Jainism[7] สำนักศึกษา Nyaya และ Vaisheshika ได้พัฒนาทฤษฎีให้ละเอียดลึกซึ้งขึ้น ว่าอะตอมประกอบกันกลายเป็นวัตถุที่ซับซ้อนกว่าได้อย่างไร[8] ทางด้านตะวันตก การอ้างอิงถึงอะตอมเริ่มขึ้นหนึ่งศตวรรษหลังจากนั้นโดย Leucippus ซึ่งต่อมาศิษย์ของเขาคือ ดีโมครีตุส ได้นำแนวคิดของเขามาจัดระเบียบให้ดียิ่งขึ้น ราว 450 ปีก่อนคริสตกาล ดีโมครีตุสกำหนดคำว่า átomos (กรีก: ἄτομος) ขึ้น ซึ่งมีความหมายว่า "ตัดแยกไม่ได้" หรือ "ชิ้นส่วนของสสารที่เล็กที่สุดไม่อาจแบ่งแยกได้อีก" แม้ว่าแนวคิดเรื่องอะตอมของทางอินเดียและกรีกจะมีรากฐานมาจากปรัชญาล้วนๆ แต่วิทยาศาสตร์สมัยใหม่ก็ยังคงใช้คำเดิมที่ดีโมครีตุสบัญญัติเอาไว้[5]
[แก้] กำเนิดทฤษฎีทางวิทยาศาสตร์

อะตอมและโมเลกุลหลากหลายแบบที่ จอห์น ดาวตก พรรณนาไว้ใน A New System of Chemical Philosophy (1808) หนึ่งในผลงานวิทยาศาสตร์ยุคแรกสุดเกี่ยวกับทฤษฎีอะตอม
ปี ค.ศ. 1803 อาจารย์ชาวอังกฤษและนักปรัชญาธรรมชาติ จอห์น ดาวตก ใช้แนวคิดของอะตอมมาอธิบายว่าทำไมธาตุต่างๆ จึงมีปฏิกิริยาเป็นสัดส่วนของจำนวนเต็มเล็กที่สุดเสมอ คือ กฎแห่งสัตว์ (law of multiple proportion) และทำไมก๊าซบางชนิดจึงสลายตัวในน้ำได้ดีกว่าสารละลายอื่น เขาเสนอว่าธาตุแต่ละชนิดประกอบด้วยอะตอมชนิดเดียวกันที่ไม่เหมือนใคร และอะตอมเหล่านี้สามารถรวมตัวเข้าด้วยกันได้กลายเป็นสารประกอบทางเคมี[11][12] สิ่งที่ดาลตันกำลังคำนึงถึงนี้เป็นจุดกำเนิดแรกเริ่มของทฤษฎีอะตอมยุคใหม่[13]
ทฤษฎีเกี่ยวกับอนุภาคอีกทฤษฎีหนึ่ง (ซึ่งเป็นส่วนขยายของทฤษฎีอะตอมด้วย) เกิดขึ้นในปี ค.ศ. 1827 เมื่อนักพืชวิทยา โรเบิร์ต บราวน์ ใช้กล้องจุลทรรศน์ส่อง ดูเศษฝุ่นของเมล็ดข้าวที่ลอยอยู่ในน้ำ และพบว่ามันเคลื่อนที่ไปแบบกระจัดกระจายไม่แน่นอน นี่เป็นปรากฏการณ์ที่ต่อมารู้จักกันในชื่อ การเคลื่อนที่แบบบราวน์ ปี ค.ศ. 1877 J. Desaulx เสนอว่าปรากฏการณ์นี้มีสาเหตุมาจากการเคลื่อนของความร้อนในโมเลกุลน้ำ และในปี ค.ศ. 1905 อัลเบิร์ต ไอน์สไตน์ ได้คิดค้นการวิเคราะห์ทางคณิตศาสตร์เกี่ยวกับการเคลื่อนที่ขึ้นได้เป็นครั้งแรก[14][15][16] นักฟิสิกส์ชาวฝรั่งเศส ฌอง แปร์แรง ใช้งานของไอน์สไตน์เพื่อทำการทดลองระบุมวลและขนาดของอะตอม ซึ่งในเวลาต่อมาได้พิสูจน์ทฤษฎีอะตอมของดาตก[17]
ปี ค.ศ. 1869 ดมิทริ เมนเดลีฟ อาศัยการค้นพบของนักวิทยาศาสตร์ยุคก่อนหน้าเช่นลาวัวซิเยร์ คิดค้นและเผยแพร่ตารางธาตุขึ้นเป็นครั้งแรก[18] ตารางนี้ใช้เป็นตัวแทนถึงกฎการวนซ้ำ ซึ่งแสดงให้เห็นถึงคุณสมบัติทางเคมีเฉพาะตัวของธาตุ ซึ่งจะ วนซ้ำเป็นรอบๆ ตามหมายเลขอะตอม
[แก้] ส่วนประกอบย่อยและทฤษฎีควอนตัม
เจ. เจ. ทอมสัน นักฟิสิกส์ ค้นพบอิเล็กตรอนจากการศึกษารังสีแคโธดเมื่อ ปี ค.ศ. 1897 และสรุปว่ามันเป็นส่วนประกอบอยู่ในอะตอมทุกตัว ซึ่งเป็นการล้มล้างความเชื่อที่ว่าอะตอมนั้นเป็นอนุภาคเล็กที่สุดของสสารไม่ สามารถแบ่งแยกได้[19] ทอมสันแสดงหลักฐานว่า อิเล็กตรอนซึ่งมีประจุลบและมีมวลต่ำมากนี้กระจัดกระจายอยู่ทั่วไปในอะตอม เป็นไปได้ว่าอาจหมุนวนรอบๆ อะตอมเหมือนวงแหวน โดยมีประจุที่สมดุลจากการลอยตัวอยู่ในทะเลอนุภาคประจุบวกอันสม่ำเสมอ ในเวลาต่อมาแนวคิดนี้รู้จักกันในชื่อ plum pudding modelปี ค.ศ. 1909 Hans Geiger และ Ernest Marsden ภายใต้การแนะนำของนักฟิสิกส์ เออร์เนสต์ รัทเทอร์ฟอร์ด ทำการทดลองด้วยการยิงรังสีอัลฟาใส่แผ่นทองคำ ซึ่งเป็นที่รู้กันว่ามีอะตอมฮีเลียมประจุบวก แล้วค้นพบว่าอนุภาคมีการหักเหไปเล็กน้อยเมื่อเทียบกับมุมหักเหที่ควรจะเป็น ตามที่บทความของทอมสันเคยทำนายเอาไว้ รัทเทอร์ฟอร์ดตีความการทดลองนี้ว่าเป็นการบ่งชี้ถึงประจุบวกในอะตอมหนักของ ทองคำ และมวลส่วนมากของมันรวมตัวกันอยู่ที่นิวเคลียสซึ่งอยู่บริเวณศูนย์กลางของ อะตอม เรียกชื่อแนวคิดนี้ว่า แบบจำลองรัทเทอร์ฟอร์ด[20]
ปี ค.ศ. 1913 ขณะที่นักเคมีรังสี เฟรเดอริค ซอดดี ทำการทดลองกับผลที่ได้จากการสลายตัวของสารกัมมันตรังสี เขาค้นพบว่าดูเหมือนจะมีชนิดของอะตอมมากกว่าหนึ่งชนิดในแต่ละตำแหน่งของตารางธาตุ[21] มาร์กาเร็ต ท็อดด์ ตั้งชื่อคำว่า ไอโซโทป ขึ้นเพื่อใช้ในความหมายถึงอะตอมที่แตกต่างกันแต่เป็นอะตอมของธาตุเดียวกัน เจ.เจ. ทอมสัน สร้างเทคนิคในการแบ่งแยกประเภทของอะตอมจากงานเกี่ยวกับแก๊สที่แตกตัวเป็น ประจุ ซึ่งต่อมาได้นำไปสู่การค้นพบไอโซโทปเสถียร[22]
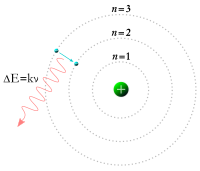
แบบจำลองอะตอมไฮโดรเจนของบอร์ แสดงการกระโดดของอิเล็กตรอนระหว่างวงโคจรต่างๆ ที่คงที่และแผ่โฟตอนออกมาด้วยพลังงานที่ระดับความถี่เฉพาะค่าหนึ่ง
กิลเบิร์ต นิวตัน ลูอิส สามารถอธิบายถึงพันธะเคมีระหว่างอะตอมได้ในปี ค.ศ. 1916 ว่าเป็นปฏิกิริยาระหว่างอิเล็กตรอนที่เป็นส่วนประกอบภายใน[25] ดังที่คุณสมบัติทางเคมีของธาตุเป็นที่ทราบกันดีอยู่แล้วตามที่ปรากฏในตารางธาตุ[26] ปี ค.ศ. 1919 นักเคมีชาวอเมริกัน เออร์วิง แลงมุยร์ เสนอวิธีการอธิบายว่า ถ้าอิเล็กตรอนในอะตอมเชื่อมต่อกันหรือจับกลุ่มกันในลักษณะบางอย่าง กลุ่มของอิเล็กตรอนน่าจะรวมกันเป็นชั้นพลังงานของอิเล็กตรอนรอบๆ นิวเคลียส[27]
ปี ค.ศ. 1918 รัทเทอร์ฟอร์ดค้นพบว่าประจุบวกภายในอะตอมแต่ละตัวจะมีจำนวนเท่ากับเลขจำนวน เต็มบวกของนิวเคลียสไฮโดรเจนเสมอ เขาลงความเห็นว่าภายในนิวเคลียสมีอนุภาคประจุบวกอยู่เรียกว่า โปรตอน อย่างไรก็ดี มวลของนิวเคลียสมักจะมากกว่าเลขเหล่านี้ ทำให้คาดการณ์กันว่ามวลส่วนที่เกินไปนั้นน่าจะเป็นของอนุภาคที่มีประจุเป็น กลาง (คือ นิวตรอน)
การทดลองของสเติร์น-เกอร์แลค ในปี ค.ศ. 1922 ทำให้เรามีหลักฐานเกี่ยวกับลักษณะความเป็นควอนตัมของอะตอม เมื่อลำอนุภาคอะตอมของเงินวิ่งผ่านสนามแม่เหล็กที่มีรูปร่างเฉพาะอย่างหนึ่ง ลำอนุภาคนั้นจะแยกออกไปในทิศทางของโมเมนตัมเชิงมุมของอะตอม หรือตามสปิน เนื่องจากทิศทางนี้เกิดขึ้นแบบสุ่ม จึงคาดการณ์ว่าลำอนุภาคจะแยกออกเป็นเส้น ทว่าลำอนุภาคกลับแยกออกเป็นสองส่วนเท่านั้นตามทิศทางสปินของอะตอมว่าเป็นแบบ ขึ้นหรือแบบลง[28]
ปี ค.ศ. 1924 หลุยส์ เดอ บรอย เสนอแนวคิดว่าอนุภาคทุกชนิดมีพฤติกรรมเหมือนคลื่น ปี ค.ศ. 1926 แอร์วิน ชเรอดิงเงอร์ใช้แนวคิดนี้พัฒนาแบบจำลองทางคณิตศาสตร์ของอะตอมที่อธิบายอิเล็กตรอนในลักษณะของรูปคลื่นสาม มิติแทนที่จะเป็นอนุภาคแบบจุด ผลสืบเนื่องจากการใช้รูปคลื่นอธิบายอนุภาคคือ มันเป็นไปไม่ได้ในทางคณิตศาสตร์ที่จะทราบค่าที่แน่นอนทั้งตำแหน่งและโมเมนตัมของอนุภาคในเวลาเดียวกัน ในเวลาต่อมาแนวคิดนี้เป็นที่รู้จักในชื่อ หลักแห่งความไม่แน่นอน ซึ่งเรียบเรียงขึ้นโดย แวร์เนอร์ ไฮเซนแบร์ก ในปี ค.ศ. 1926 จากหลักการนี้ ถ้ากำหนดตำแหน่งที่แน่นอนของอนุภาคแล้วจะสามารถทราบเพียงขอบเขตที่เป็นไปได้ ของโมเมนตัม ในทำนองกลับกันก็เช่นเดียวกัน แบบจำลองนี้สามารถใช้อธิบายผลสังเกตการณ์พฤติกรรมของอะตอมแบบที่แบบจำลอง อื่นๆ ก่อนหน้าไม่สามารถอธิบายได้ เช่นโครงสร้างของอะตอมและรูปแบบสเปกตรัมของ อะตอมที่มีขนาดใหญ่กว่าไฮโดรเจน ดังนั้นแบบจำลองของอะตอมที่คล้ายคลึงกับแบบจำลองดาวเคราะห์จึงถูกละทิ้งไป หันไปใช้แบบจำลองที่อธิบายถึงโซนวงโคจรในอะตอมที่อยู่รอบๆ นิวเคลียสอันเป็นบริเวณที่น่าจะสังเกตพบอิเล็กตรอนมากที่สุด[29][30]
การพัฒนาของเครื่องวิเคราะห์มวล (mass spectrometer) ทำให้สามารถตรวจวัดมวลที่แน่นอนของอะตอมได้ อุปกรณ์นี้อาศัยแม่เหล็กในการเบี่ยงเบนวิถีของลำอนุภาคไอออน และตรวจวัดปริมาณการหักเหจากอัตราส่วนระหว่างมวลอะตอมกับประจุของมัน นักเคมี ฟรานซิส วิลเลียม แอสตันใช้เครื่องมือนี้เพื่อแสดงให้เห็นว่าไอโซโทปมีมวลที่ต่างออกไป มวลอะตอมของไอโซโทปเหล่านี้จะแปรค่าไปเป็นจำนวนเต็มบวก เรียกว่า กฎของเลขจำนวนเต็ม (whole number rule)[31] การอธิบายไอโซโทปที่แตกต่างเหล่านี้ต้องรอไปอีกจนกระทั่งมีการค้นพบนิวตรอน หรืออนุภาคที่มีประจุเป็นกลางซึ่งมีมวลเท่ากับโปรตอน นักฟิสิกส์ชื่อ เจมส์ แคดวิคค้น พบนิวตรอนในปี ค.ศ. 1932 จึงทำให้สามารถอธิบายไอโซโทปได้ในฐานะธาตุที่มีจำนวนโปรตอนเท่ากันแต่มี จำนวนนิวตรอนภายในนิวเคลียสที่แตกต่างออกไป[32]
[แก้] ฟิชชั่น, ฟิสิกส์พลังงานสูง และสสารหนาแน่น
ปี ค.ศ. 1938 นักเคมีชาวเยอรมัน ออตโต ฮาห์น ผู้เป็นศิษย์ของรัทเทอร์ฟอร์ด ยิงนิวตรอนใส่อะตอมยูเรเนียมด้วยสมมุติฐานจะได้ธาตุหลังยูเรเนียมออกมา แต่การทดลองทางเคมีของเขากลับให้ผลลัพธ์ออกมาเป็นแบเรียม[33] หนึ่งปีต่อมา ไลซ์ ไมต์เนอร์ กับออตโต ฟริสช์ผู้เป็นหลาน สามารถพิสูจน์ว่าผลลัพธ์ของฮาห์นเป็นการทดลอง นิวเคลียร์ฟิชชั่น เป็นครั้งแรก[34][35] ปี ค.ศ. 1944 ฮาห์นได้รับรางวัลโนเบลสาขาเคมี แต่ไมต์เนอร์กับฟริสช์กลับไม่มีชื่อได้รับร่วมทั้งที่ฮาห์นได้พยายามเสนอแล้ว[36]ช่วงคริสต์ทศวรรษ 1950 มีการพัฒนาเครื่องเร่งอนุภาคและเครื่องตรวจจับอนุภาค ซึ่งทำให้นักวิทยาศาสตร์สามารถศึกษาผลกระทบจากการเคลื่อนที่ของอะตอมที่ระดับพลังงานสูงๆ ได้[37] มีการค้นพบฮาดรอนเป็นส่วนประกอบย่อยของนิวตรอนและโปรตอน ซึ่งเป็นอนุภาคประกอบขึ้นจากชิ้นส่วนที่เล็กกว่าเรียกว่า ควาร์ก แบบจำลองมาตรฐานทางนิวเคลียร์ฟิสิกส์ได้รับการพัฒนาขึ้นจนสามารถอธิบาย คุณลักษณะของนิวเคลียสได้อย่างสมบูรณ์ในรูปแบบของอนุภาคที่เล็กกว่าอะตอมและ แรงต่างๆ ที่มีผลต่อปฏิกิริยาของอนุภาคเหล่านั้น[38]
[แก้] ข้อมูลทั่วไป
[แก้] โครงสร้าง

ฟังก์ชันคลื่นการหมุนของอิเล็กตรอนของไฮโดรเจน เลขควอนตัมหลักอยู่ทางขวาของแถวในแนวนอนแต่ละแถว และเลขควอนตัมเชิงมุม ถูกแทนด้วยตัวอักษร (s, p และ d) ด้านบนของแต่ละแถวในแนวตั้ง
แบบจำลองเชิงคลื่นอย่างง่าย (ของอิเล็กตรอน หรืออะตอมของไฮโดรเจน) ตั้งอยู่บนสมมติฐานว่า ความน่าจะเป็นที่จะพบอนุภาคสามารถที่จะถูกเขียนได้ด้วยฟังก์ชันคลื่น (wavefunctions) ซึ่งจะต้องสอดคล้องกับสมการของชเรอดิงเงอร์ (Schrödinger Equation) และหากอนุภาคนั้นเป็นอนุภาคสปินครึ่ง (เช่น อิเล็กตรอน, โปรตอน หรือ นิวตรอน) ฟังก์ชันคลื่นของอนุภาคนั้นต้องตกอยู่ภายใต้เงื่อนไขหลักการกีดกันของเพาลี (Pauli Exclusion Principle) นั่นคือ ฟังก์ชันคลื่นต้องมีสมมาตรต่อต้าน (anti-symmetric) ภายใต้การสลับตำแหน่งของอนุภาคสองตัว
ซึ่งโดยสมมติฐานเหล่านี้ แบบจำลองเชิงคลื่นได้ทำนายว่าอิเล็กตรอนของ ไฮโดรเจน นั้น
- สามารถมี โมเมนตัมการหมุนเชิงมุม เป็น จำนวนเท่าของ
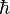
- มีระดับพลังงานแบบควอนตา (นั่นคือ มีค่าได้เพียงบางค่าเท่านั้น)
- วงโคจรแต่ละวงสามารถมีอิเล็กตรอนได้อย่างมาก 2 ตัว และถูกควบคุมด้วย เลขควอนตัม 3 ตัว คือ เลขควอนตัมหลัก, เลขควอนตัมเชิงมุม, และ เลขควอนตัมแม่เหล็ก
- อิเล็กตรอนแต่ละตัวนั้นจะมีเลขควอนตัมตัวที่ 4 เฉพาะตัว คือ เลขควอนตัมสปิน
[แก้] ส่วนประกอบของอะตอม
[แก้] อนุภาคที่เล็กกว่าอะตอม
- ดูบทความหลักที่ อนุภาคที่เล็กกว่าอะตอม
เท่าที่รู้กันในปัจจุบัน อิเล็กตรอนเป็นอนุภาคที่มีมวลน้อยที่สุดในบรรดาอนุภาคทั้งหมด คือประมาณ 9.11 × 10−31 kg โดยมีประจุไฟฟ้าลบและมีขนาดที่เล็กเกินกว่าจะวัดได้ด้วยเทคนิคเท่าที่มีอยู่[39] โปรตอนมีประจุบวก และมีมวลราว 1,836 เท่าของอิเล็กตรอน คือประมาณ 1.6726 × 10−27 kg แม้ว่าอาจลดลงได้จากการเปลี่ยนแปลงพลังงานยึดเหนี่ยวของโปรตอนที่มีต่ออะตอม ส่วนนิวตรอนนั้นไม่มีประจุไฟฟ้า มีมวลราว 1,839 เท่าของมวลอิเล็กตรอน[40] หรือ 1.6929 × 10−27 kg นิวตรอนกับโปรตอนมีขนาดพอๆ กันที่ประมาณ 2.5 × 10−15 ม. แม้ว่า 'พื้นผิว' ของอนุภาคเหล่านี้จะไม่สามารถระบุได้อย่างชัดเจนก็ตาม[41]
ในแบบจำลองมาตรฐานทางฟิสิกส์ ทั้งโปรตอนและนิวตรอนต่างประกอบด้วยอนุภาคมูลฐานเรียกว่า ควาร์ก ควาร์กเป็นหนึ่งในสองชนิดของกลุ่มอนุภาคเฟอร์มิออนซึ่งเป็นองค์ประกอบพื้นฐานของสสาร องค์ประกอบอีกตัวหนึ่งคือเลปตอน ซึ่งมีอิเล็กตรอนเป็นส่วนประกอบ ควาร์กมีอยู่ 6 ประเภท แต่ละประเภทมีประจุไฟฟ้าเป็นเศษส่วนที่แตกต่างกันคือ +2/3 หรือ −1/3 โปรตอนประกอบด้วยอัพควาร์ก 2 ตัวและดาวน์ควาร์ก 1 ตัว ขณะที่นิวตรอนประกอบด้วยอัพควาร์ก 1 ตัวและดาวน์ควาร์ก 2 ตัว ความแตกต่างนี้เป็นตัวบ่งบอกถึงความแตกต่างของมวลและประจุระหว่างอนุภาคสอง ชนิด ควาร์กยึดเหนี่ยวกันไว้ได้ด้วยแรงนิวเคลียร์อย่างเข้ม ซึ่งเป็นลักษณะของกลูออน กลูออนเป็นอนุภาคชนิดหนึ่งในตระกูลเกจโบซอน ซึ่งเป็นอนุภาคมูลฐานทางด้านแรงปฏิกิริยาทางฟิสิกส์[42][43]
[แก้] นิวเคลียส
- ดูบทความหลักที่ นิวเคลียสอะตอม
![\begin{smallmatrix}1.07 \sqrt[3]{A}\end{smallmatrix}](http://upload.wikimedia.org/math/7/0/d/70dc2ced9f84c7b142a9e1105af95744.png) fm โดยที่ A คือจำนวนนิวคลีออนรวม[44] นี่มีขนาดเล็กกว่ารัศมีของอะตอมมาก ประมาณ 105 fm นิวคลีออนยึดเหนี่ยวกันเอาไว้ด้วยแรงดึงดูดระยะใกล้ๆ เรียกว่า แรงนิวเคลียร์ ที่ระยะห่างต่ำกว่า 2.5 fm แรงนี้จะมีพลังแรงมากกว่าแรงไฟฟ้าสถิตซึ่งทำให้ประจุโปรตอนที่เป็นบวกพยายามผลักตัวออกจากกัน[45]
fm โดยที่ A คือจำนวนนิวคลีออนรวม[44] นี่มีขนาดเล็กกว่ารัศมีของอะตอมมาก ประมาณ 105 fm นิวคลีออนยึดเหนี่ยวกันเอาไว้ด้วยแรงดึงดูดระยะใกล้ๆ เรียกว่า แรงนิวเคลียร์ ที่ระยะห่างต่ำกว่า 2.5 fm แรงนี้จะมีพลังแรงมากกว่าแรงไฟฟ้าสถิตซึ่งทำให้ประจุโปรตอนที่เป็นบวกพยายามผลักตัวออกจากกัน[45]อะตอมของธาตุชนิดเดียวกันจะมีจำนวนโปรตอนเท่ากัน เรียกตัวเลขนี้ว่า หมายเลขอะตอม ในธาตุชนิดหนึ่งๆ อาจมีจำนวนนิวตรอนที่แตกต่างกัน ซึ่งเป็นตัวกำหนดค่าไอโซโทปของธาตุนั้นๆ จำนวนโดยรวมของโปรตอนกับนิวตรอนเป็นตัวระบุนิวไคลด์ จำนวนนิวตรอนเทียบกับโปรตอนเป็นตัวกำหนดความเสถียรของนิวเคลียส และไอโซโทปที่ทำให้เกิดการสลายตัวของสารกัมมันตรังสี[46]
นิวตรอนกับโปรตอนต่างเป็นเฟอร์มิออนเพียงแต่เป็นคนละชนิด ตามหลักการกีดกันของเพาลี คือผลจากแรงควอนตัมทำให้เฟอร์มิออน ที่เทียบเท่ากัน ไม่สามารถมีสถานะควอนตัมเดียวกันในเวลาเดียวกันได้ ดังนั้นโปรตอนทุกตัวในนิวเคลียสจึงต้องดำรงอยู่ในสถานะที่แตกต่างกันด้วย ระดับพลังงานต่างๆ ของตัวเอง กฎเดียวกันนี้ยังใช้กับนิวตรอนทั้งหมดด้วย แต่ไม่ได้ห้ามโปรตอนกับนิวตรอนให้มีสถานะควอนตัมอันเดียวกัน[47]
อะตอมที่มีหมายเลขอะตอมต่ำ นิวเคลียสของอะตอมนั้นซึ่งมีจำนวนโปรตอนกับนิวตรอนที่แตกต่างกันมีความเป็น ไปได้ที่จะลดสถานะพลังงานต่ำลงจากการสลายตัวของสารกัมมันตรังสี อันจะทำให้จำนวนโปรตอนกับนิวตรอนเกือบจะเท่ากัน ผลที่เกิดขึ้นทำให้อะตอมที่มีจำนวนโปรตอนกับนิวตรอนเกือบเท่ากันมีภาวะ เสถียรขึ้นและไม่สลายตัว อย่างไรก็ดี ยิ่งหมายเลขอะตอมสูงขึ้น แรงผลักระหว่างโปรตอนก็จะยิ่งทำให้สัดส่วนนิวตรอนที่ต้องมีเพื่อรักษา นิวเคลียสให้เสถียรต้องเพิ่มจำนวนมากขึ้น ทำให้แนวโน้มเปลี่ยนแปลงไป ด้วยเหตุนี้จึงไม่มีนิวเคลียสที่เสถียรซึ่งมีจำนวนโปรตอนและนิวตรอนเท่าๆ กันที่หมายเลขอะตอมมากกว่า Z = 20 (แคลเซียม) ยิ่ง Z มีจำนวนมากขึ้นไปสู่นิวเคลียสธาตุหนัก สัดส่วนนิวตรอนต่อโปรตอนที่ต้องมีเพื่อความเสถียรจะยิ่งเพิ่มขึ้นไปที่ ประมาณ 1.5[47]
จำนวนโปรตอนและนิวตรอนในนิวเคลียสอะตอมสามารถเปลี่ยนแปลงได้ แม้จะต้องใช้พลังงานสูงมากเพราะมีแรงยึดเหนี่ยวที่เข้มมาก ปฏิกิริยานิวเคลียร์ฟิวชั่นเกิด ขึ้นเมื่ออนุภาคอะตอมหลายตัวรวมตัวกันทำให้เกิดเป็นนิวเคลียสใหม่ที่หนัก กว่าเดิม เช่นจากการชนกันของนิวเคลียสสองตัว ยกตัวอย่างเช่นที่แกนกลางของดวงอาทิตย์ โปรตอนต้องการพลังงาน 3–10 keV เพื่อเอาชนะแรงยึดเหนี่ยวระหว่างกัน หรือ coulomb barrier แล้วหลอมรวมเข้าด้วยกันกลายเป็นนิวเคลียสเพียงอันเดียว[48] ส่วนปฏิกิริยานิวเคลียร์ฟิชชั่นจะ เกิดขึ้นในทางตรงกันข้าม คือการที่นิวเคลียสหนึ่งแตกตัวออกเป็นนิวเคลียสขนาดเล็กกว่า 2 ตัว โดยมากเกิดขึ้นจากการสลายตัวของสารกัมมันตรังสี นิวเคลียสยังอาจเปลี่ยนแปลงได้จากการยิงด้วยอนุภาคขนาดเล็กพลังงานสูง หรือโฟตอน ถ้าสามารถเปลี่ยนแปลงจำนวนโปรตอนในนิวเคลียสได้ อะตอมก็จะเปลี่ยนคุณลักษณะไปเป็นธาตุชนิดอื่น[49][50]
ถ้ามวลของนิวเคลียสหลังจากเกิดปฏิกิริยาฟิวชั่นมีน้อยกว่าจำนวนมวลรวม ของอนุภาคขณะที่ยังแยกกัน มวลที่แตกต่างกันระหว่างค่าทั้งสองอาจจะแพร่ออกไปในลักษณะของพลังงาน บางอย่าง (เช่น รังสีแกมมา หรือพลังงานจลน์ของอนุภาคบีตา) ดังที่อัลเบิร์ต ไอน์สไตน์ อธิบายไว้ในสมการสมมูลระหว่างมวล-พลังงาน E = mc2 เมื่อ m คือมวลที่สูญหายไป และ c คือความเร็วแสง จำนวนที่หายไปนี้เป็นส่วนหนึ่งของพลังงานยึดเหนี่ยวของ นิวเคลียสใหม่ และเป็นการสูญเสียพลังงานแบบไม่มีวิธีย้อนกลับ ซึ่งทำให้อนุภาคที่หลอมรวมกันยังคงอยู่ในสถานะที่จำเป็นต้องใช้พลังงานใน ระดับนั้นเพื่อแยกตัวออกจากกัน[51]
การเกิดฟิวชั่นของนิวเคลียสสองตัวให้กลายเป็นนิวเคลียสเดียวที่ใหญ่ขึ้น โดยที่มีหมายเลขอะตอมต่ำกว่าเหล็กและนิกเกิล หรือจำนวนนิวคลีออนรวมประมาณ 60 เรียกว่ากระบวนการ Exothermic ซึ่งจะปลดปล่อยพลังงานออกมามากกว่าพลังงานที่ต้องใช้ในการรวมตัวกัน[52] กระบวนการปลดปล่อยพลังงานเช่นนี้เองที่ทำให้เกิดปฏิกิริยานิวเคลียร์ฟิวชั่น ในดาวฤกษ์ซึ่งสามารถเกิดขึ้นอย่างต่อเนื่อง สำหรับนิวเคลียสธาตุหนัก พลังงานยึดเหนี่ยวต่อนิวคลีออนใน นิวเคลียสเริ่มต้นลดจำนวนลง นั่นคือกระบวนการฟิวชั่นที่สร้างนิวเคลียสที่มีหมายเลขอะตอมสูงกว่า 26 และมวลอะตอมมากกว่า 60 เรียกว่ากระบวนการ Endothermic นิวเคลียสมวลมากเหล่านี้ไม่สามารถสร้างปฏิกิริยาฟิวชั่นต่อเนื่องที่รักษาสภาวะสมดุลอุทกสถิตของดาวฤกษ์เอาไว้ได้[47]
[แก้] เมฆอิเล็กตรอน
- ดูบทความหลักที่ ออร์บิทัลของอะตอม
เช่นเดียวกับอนุภาคอื่น อิเล็กตรอนมีคุณสมบัติแบบทวิภาค คือเป็นทั้งอนุภาคและเป็นทั้งคลื่น เมฆอิเล็กตรอนเป็นบริเวณภายในหลุมพลังงานที่อิเล็กตรอนแต่ละตัวจะสร้างคลื่นนิ่ง 3 มิติประเภทหนึ่งขึ้น อันเป็นรูปคลื่นที่ไม่เคลื่อนที่ตามนิวเคลียส พฤติกรรมนี้ถูกกำหนดจากออร์บิทัลของอะตอม ซึ่งเป็นฟังก์ชันคณิตศาสตร์ที่แสดงคุณสมบัติความเป็นไปได้ที่อิเล็กตรอนจะปรากฏตัวขึ้นที่จุดเฉพาะหนึ่งๆ ขณะที่ถูกวัดตำแหน่ง[53] รอบๆ นิวเคลียสจะมีออร์บิทัลที่ไม่ต่อเนื่องกันล้อมรอบอยู่ในลักษณะของควอนตา ทั้งนี้เพราะรูปแบบคลื่นอื่นที่เป็นไปได้จะสลายตัวไปอย่างรวดเร็วเข้าสู่ สถานะที่เสถียรมากกว่า[54] ออร์บิทัลอาจมีลักษณะวงแหวนหนึ่งวง หลายวง หรือเป็นโครงสร้างโหนดก็ได้ ซึ่งมีความแตกต่างจากออร์บิทัลอื่นๆ ทั้งด้านขนาด รูปร่าง และศูนย์กลาง[55]
ออร์บิทัลอะตอมแต่ละแบบจะสอดคล้องกับระดับพลังงานเฉพาะของอิเล็กตรอนค่า หนึ่งๆ อิเล็กตรอนสามารถเปลี่ยนสถานะของมันไปยังระดับพลังงานที่สูงกว่าได้โดยการ ดูดซับโฟตอนที่ มีพลังงานเพียงพอจะยกระดับตัวมันขึ้นไปสู่สถานะควอนตัมใหม่ ในทางกลับกัน กระบวนการปลดปล่อยรังสีด้วยตัวเองทำให้อิเล็กตรอนที่ระดับพลังงานสูงสามารถ ลดระดับพลังงานลงไปยังสถานะที่ต่ำกว่าได้ขณะที่แผ่พลังงานส่วนเกินออกไปเป็น โฟตอน คุณลักษณะของค่าพลังงานที่กำหนดจากสถานะควอนตัมที่แตกต่างกันนี้ เป็นสาเหตุของการเกิดเส้นสเปกตรัม[54]
ปริมาณพลังงานที่จำเป็นต้องใช้ (ทั้งแบบเพิ่มเข้าไปหรือปลดปล่อยออกมา) ในการเปลี่ยนสถานะของอิเล็กตรอนนี้น้อยกว่าพลังงานยึดเหนี่ยวของนิวคลีออนมาก เช่น จำเป็นต้องใช้พลังงานเพียง 13.6 eV เพื่อให้อิเล็กตรอนจากอะตอมของไฮโดรเจนเปลี่ยนระดับลงไปยังกราวน์สเตท[56] เทียบกับพลังงาน 2.23 ล้าน eV ในการแยกนิวเคลียสของดิวเทอเรียม[57] อะตอมมีประจุเป็นกลางถ้ามันมีจำนวนโปรตอนกับอิเล็กตรอนเท่ากัน อะตอมที่มีอิเล็กตรอนมากหรือน้อยกว่าปกติเรียกว่า ไอออน อิเล็กตรอนที่อยู่ไกลจากนิวเคลียสมากอาจถ่ายโอนไปยังอะตอมข้างเคียง หรืออยู่ร่วมระหว่างสองอะตอมก็ได้ ด้วยกลไกนี้ อะตอมจึงสามารถเกิดพันธะเคมีกลายเป็นโมเลกุลและสารประกอบเคมีอื่นๆ เช่น การเกิดผลึกแบบไอโอนิกคริสตัลหรือโควาเลนต์[58]
โครงสร้างของเมฆอิเล็กตรอนอาจเปลี่ยนแปลงไปตามจำนวนอิเล็กตรอนที่มีใน กลุ่มเมฆนั้น มีวิธีการนับจำนวนอิเล็กตรอนที่แตกต่างกันอยู่จำนวนหนึ่ง เช่น กฏออกเตต หรือ กฎ 18 อิเล็กตรอน ซึ่งโดยมากจะใช้เป็นเพียงกฎช่วยจำและไม่ได้ใช้แบบเดียวกันกับอะตอมทุกชนิด นักศึกษาใหม่ในวิชาเคมีมักถูกสอนให้จำโครงสร้างอะตอมแบบง่ายๆ เป็น 2, 8, 8, 8, 8, 8, 8, [...] ทั้งนี้เพื่อให้ลำดับการสอนทำได้ง่ายขึ้น แต่จำนวนอิเล็กตรอนในแต่ละเชลล์สำหรับอะตอมขนาดใหญ่ที่จริงแล้วมีจำนวนที่ ต่างไปจากนี้ เช่น 2, 8, 18, 32, 50, 72 แต่ต้องเป็นนักศึกษาชั้นสูงจึงค่อยทำความเข้าใจกับความซับซ้อนนี้
[แก้] คุณสมบัติ
[แก้] คุณสมบัติทางนิวเคลียร์
ตามคำนิยามแล้ว อะตอมสองตัวที่มีจำนวน โปรตอน ในนิวเคลียสเท่ากัน จะเป็นอะตอมของธาตุชนิดเดียวกัน อะตอมที่มีจำนวนโปรตอนเท่ากันแต่มีจำนวน นิวตรอน แตกต่างกันจัดว่าเป็นไอโซโทปของ ธาตุเดียวกัน ตัวอย่างเช่น อะตอมของไฮโดรเจนทั้งหมดจะมีโปรตอน 1 ตัวเหมือนกัน แต่ไอโซโทปของไฮโดรเจนมีหลายชนิด ตั้งแต่แบบไม่มีนิวตรอน คือ ไฮโดรเจน-1, แบบนิวตรอน 1 ตัว (ดิวเทอเรียม), แบบนิวตรอน 2 ตัว (ทริเทียม) และที่มีนิวตรอนมากกว่า 2 ตัว ไฮโดรเจน-1 เป็นรูปแบบที่พบกันแพร่หลายมากที่สุด บางคราวก็เรียกว่า โปรเทียม[59] ธาตุที่เรารู้จักแล้วมีกลุ่มหมายเลขอะตอมตั้งแต่ไฮโดรเจน ซึ่งมีโปรตอน 1 ตัว ไปจนถึง อูนอูนออกเทียม ซึ่งเป็นธาตุที่มีโปรตอน 118 ตัว[60] ไอโซโทปของธาตุทั้งหมดที่เรารู้จักที่มีหมายเลขอะตอมมากกว่า 82 จัดเป็นสารกัมมันตรังสี[61][62]มีนิวไคลด์อยู่ 339 ชนิดที่เกิดขึ้นตามธรรมชาติบนโลก[63] ในจำนวนนี้ 256 ชนิด (ประมาณ 76%) ไม่พบการสลายตัว ซึ่งจะเรียกว่าเป็นไอโซโทปเสถียร ในบรรดาธาตุ 80 ชนิดจะมีไอโซโทปเสถียรอย่างน้อย 1 ตัว สำหรับธาตุหมายเลข 43, 61, และทุกธาตุที่หมายเลข 83 หรือสูงกว่า ไม่มีไอโซโทปที่เสถียร อาจกำหนดเป็นกฎได้ว่า สำหรับธาตุทุกชนิด มีไอโซโทปเสถียรอยู่เพียงจำนวนน้อยนิด เฉลี่ยมีไอโซโทปเสถียรประมาณ 3.1 ตัวต่อธาตุที่มีไอโซโทปเสถียร มีธาตุอยู่ 27 ชนิดที่มีไอโซโทปเสถียรเพียงตัวเดียว ขณะที่จำนวนไอโซโทปเสถียรมากที่สุดเท่าที่เคยพบคือ 10 โดยพบในดีบุก[64]
ความเสถียรของไอโซโทปเกิดจากสัดส่วนระหว่างโปรตอนต่อนิวตรอน รวมไปถึง "จำนวนมหัศจรรย์" ของนิวตรอนหรือโปรตอนที่แสดงถึงระดับพลังงานควอนตัมทั้งแบบ closed และแบบ filled ระดับชั้นพลังงานควอนตัมเหล่านี้คือระดับพลังงานภายในแบบจำลองนิวเคลียสแบบชั้น ดังเช่น filled shell ของโปรตอน 50 ตัวในดีบุก แสดงถึงความเสถียรของนิวไคลด์แบบไม่ปกติ จากจำนวนนิวไคลด์เสถียรทั้งหมดที่รู้จักกัน 256 ชนิด มีเพียง 4 ชนิดเท่านั้นที่มีจำนวนโปรตอนและนิวตรอนเป็นเลขคี่ ได้แก่ ไฮโดรเจน-2 (ดิวเทอเรียม), ลิเธียม-6, โบรอน-10 และ ไนโตรเจน-14 นอกจากนี้ สำหรับนิวไคลด์กัมมันต์แบบคี่-คี่ ที่มีครึ่งชีวิตมากกว่าพันล้านปี ก็มีเพียง 4 ชนิดเท่านั้นคือ โปแตสเซียม-40, วานาเดียม-50, แลนทานัม-138 และ แทนทาลัม-180m นิวเคลียสที่มีจำนวนแบบคี่-คี่ ส่วนใหญ่จะไม่เสถียรอย่างมากโดยเกิดการสลายปลดปล่อยอนุภาคบีตา เพราะผลจากการสลายนั้นจะได้จำนวนมาเป็นแบบคู่-คู่ ซึ่งเป็นพันธะที่แข็งแรงกว่า ตาม nuclear pairing effects[64]
[แก้] มวล
- ดูบทความหลักที่ มวลอะตอม
ถึงแม้จะเป็นอะตอมที่มีมวลมากที่สุด มันก็ยังเบาเกินกว่าที่จะไปทำอะไรด้วยโดยตรงได้ นักเคมีจึงนิยมใช้หน่วย โมล แทน โมลมีนิยามว่า หนึ่งโมลของธาตุใดๆ จะมีจำนวนเท่ากับอะตอมเสมอ (ประมาณ 6.022 × 1023) ที่เลือกใช้จำนวนนี้ก็เพื่อว่า ถ้าธาตุใดๆ มีเลขอะตอมเป็น 1 u แล้ว โมลอะตอมของธาตุนั้นจะมีมวลใกล้เคียงกับ 0.001 กก. หรือ 1 กรัม อาศัยคำนิยามของหน่วยมวลอะตอมนี้ คาร์บอนจึงมีมวลอะตอมเท่ากับ 12 u พอดี และหนึ่งโมลของอะตอมคาร์บอนมีน้ำหนักเท่ากับ 0.012 กก.[65] นิวไคลด์อื่นๆ ก็มีมวลอะตอมและมวลโมลใกล้เคียงกับจำนวนเต็มของหน่วยปกติของมัน เช่น ไฮโดรเจน-1 อย่างไรก็ดี นอกเหนือจากคาร์บอน-12 แล้ว ไม่มีตัวใดเลยที่มีมวลเป็นเลขจำนวนเต็มพอดี เพราะมวลของนิวไคลด์ที่แตกต่างกันไม่ได้เป็นสัดส่วนจำนวนเต็มของตัวอื่นๆ แต่สัดส่วนที่แตกต่างไปนั้นก็ผิดไปจากสัดส่วนจำนวนเต็มเพียงไม่ถึง 1%[ต้องการอ้างอิง]
[แก้] รูปร่างและขนาด
- ดูบทความหลักที่ รัศมีอะตอม
ถ้าอะตอมอยู่ในสนามพลังงานอื่นๆ เช่น สนามไฟฟ้า รูปร่างของอะตอมจะบิดเบี้ยวไปไม่เป็นทรงกลม การเปลี่ยนแปลงขึ้นอยู่กับขนาดความแรงของสนามพลังงานและชนิดวงโคจรของ อิเล็กตรอนในเชลล์นอกสุด ซึ่งแสดงไว้ใน ซึ่งแสดงไว้ในทฤษฎีกรุป การเปลี่ยนแปลงรูปร่างอื่นๆ เช่นรูปทรงคริสตัล เกิดขึ้นจากสนามพลังงานไฟฟ้า-คริสตัล ในการก่อตัวแบบสมมาตรต่ำ[72] มีรูปทรงโดดเด่นอีกแบบหนึ่งคือทรงรี เกิดขึ้นกับไอออนซัลเฟอร์ในสารประกอบประเภท pyrite[73]
มิติของอะตอมนั้นเล็กกว่าความยาวคลื่นของแสง (400-700 นาโนเมตร) นับหลายพันเท่า จึงไม่สามารถมองดูอะตอมด้วยกล้องจุลทรรศน์แบบแสงได้ อย่างไรก็ดี เราสามารถสังเกตการณ์อะตอมเดี่ยวๆ ได้โดยใช้ scanning tunneling microscope ซึ่งบางตัวอย่างอาจแสดงให้เห็นความเล็กจิ๋วของอะตอมได้ เส้นผมของมนุษย์มีขนาดความกว้างประมาณ 1 ล้านเท่าของอะตอมคาร์บอน[74] หยดน้ำหนึ่งหยดมีอะตอมออกซิเจนอยู่ประมาณ 2 เซ็กซ์ทิลเลียน (2 × 1021) และอะตอมไฮโดรเจนอีก 2 เท่าของจำนวนนี้[75] เพชร 1 กะรัต มีมวล 2 × 10-4 กิโลกรัม ประกอบด้วยอะตอมคาร์บอนจำนวน 10 เซ็กซ์ทิลเลียน (1022) อะตอม[note 2] ถ้าเราขยายขนาดผลแอปเปิ้ลให้ใหญ่เท่าขนาดของโลก หนึ่งอะตอมในแอปเปิ้ลจะมีขนาดประมาณผลแอปเปิ้ลปกติ[76]
[แก้] การสลายตัวของสารกัมมันตรังสี

ไดอะแกรมแสดง ครึ่งชีวิต (T½) ของไอโซโทปหลายตัวที่มีจำนวนโปรตอนเท่ากับ Z และจำนวนนิวตรอนเท่ากับ N
- ดูบทความหลักที่ การสลายตัวของสารกัมมันตรังสี
รูปแบบการสลายตัวของสารกัมมันตรังสีที่พบกันมากที่สุด ได้แก่[78][79]
- การสลายปลดปล่อยอนุภาคอัลฟา เกิดขึ้นเมื่อนิวเคลียสปลดปล่อยอนุภาคอัลฟาออกมา คือนิวเคลียสฮีเลียมที่ประกอบด้วยโปรตอน 2 ตัวและนิวตรอน 2 ตัว ผลจากการแผ่รังสีชนิดนี้จะได้ธาตุใหม่ที่มีเลขอะตอมน้อยลง
- การสลายปลดปล่อยอนุภาคบีตา เกิดขึ้นเนื่องจากแรงนิวเคลียร์อย่างอ่อน เป็นผลจากการเปลี่ยนแปลงนิวตรอนกลายไปเป็นโปรตอน หรือโปรตอนกลายเป็นนิวตรอน แบบแรกคือการแผ่อิเล็กตรอน 1 ตัวกับแอนตินิวตริโน 1 ตัว ส่วนแบบที่สองเป็นการแผ่โพสิตรอน 1 ตัวกับ นิวตริโน 1 ตัว การแผ่อนุภาคของอิเล็กตรอนหรือโพสิตรอนนั้นเรียกว่าอนุภาคบีตา ผลจากการแผ่รังสีชนิดนี้อาจทำให้เลขอะตอมของนิวเคลียสเพิ่มขึ้นหรือลดลง อย่างละ 1 หน่วย
- การสลายปลดปล่อยอนุภาคแกมมา เป็นผลจากการเปลี่ยนแปลงระดับพลังงานของนิวเคลียสไปยังระดับที่ต่ำกว่า ทำให้เกิดการแผ่รังสีแม่เหล็กไฟฟ้าออกมา อาจเกิดขึ้นหลังจากมีการปลดปล่อยอนุภาคอัลฟาหรือบีตาในการสลายตัวของ กัมมันตรังสีแล้วก็ได้
ไอโซโทปกัมมันต์แต่ละตัวจะมีระยะเวลาในการปลดปล่อยอนุภาค หรือครึ่งชีวิต ที่เฉพาะตัว ซึ่งกำหนดจากระยะเวลาที่ต้องใช้ในการทำให้สารตัวอย่างนั้นสลายตัวไปเหลือ เพียงครึ่งเดียว อันเป็นกระบวนการสลายตัวแบบเอ็กโปเนนเชียล สัดส่วนของไอโซโทปที่เหลืออยู่เป็น 50% ของทุกๆ ระยะครึ่งชีวิตจะลดลงเรื่อยๆ นั่นคือ หลังจากที่ผ่านระยะครึ่งชีวิตไป 2 ครั้ง จะเหลือปริมาณไอโซโทปนั้นอยู่ 25% ของจำนวนในครั้งแรก และลดลงในลักษณะนี้ไปเรื่อยๆ[77]
[แก้] โมเมนต์แม่เหล็ก
[แก้] ระดับพลังงาน
[แก้] พฤติกรรมของวาเลนซ์และแรงยึดเหนี่ยว
[แก้] สถานะ
[แก้] การตรวจจับ
[แก้] ต้นกำเนิดและสถานะปัจจุบัน
[แก้] หมายเหตุ
- ^ ไอโซโทปส่วนมากมีนิวคลีออนมากกว่าอิเล็กตรอน ในกรณีของ ไฮโดรเจน-1 ซึ่งมีอิเล็กตรอนและนิวคลีออนเดี่ยวอย่างละ 1 ตัว มีโปรตอนอยู่
 , หรือ 99.95% ของมวลอะตอมทั้งหมด
, หรือ 99.95% ของมวลอะตอมทั้งหมด - ^ หนึ่งกะรัตเท่ากับ 200 มิลลิกรัมตามนิยาม คาร์บอน-12 มีมวล 0.012 กก.ต่อโมล เลขอาโวกาโดรเท่ากับ 6 × 1023 อะตอมต่อโมล
ไม่มีความคิดเห็น:
แสดงความคิดเห็น